Når man hører på nyhetene om at et legemiddel er for dyrt for Norge, hva betyr egentlig det? Hva og hvem er det som avgjør at der for dyrt? Hvordan bestemmes det at ett legemiddel blir betalt for av det offentlige helsevesenet, mens andre legemidler ikke blir det? Hvordan blir et legemiddel godkjent og hvordan avgjøres det hvem som skal få bruke det etter godkjennelse? Hvorfor tar det egentlig så lang tid før norske pasienter får tilgang til nye medisiner?
Se den forklarende skriblefilmen om det norske systemet for tilgang til nye medisiner her.
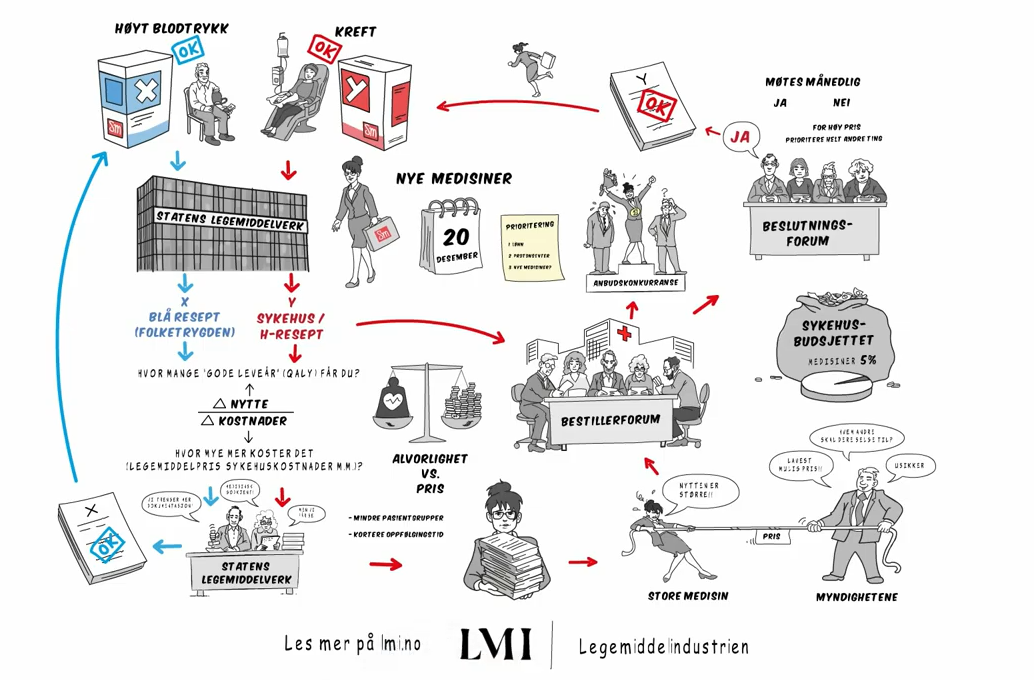
Flere av disse spørsmålene stilles hver dag, og for å få svaret, må vi ta et dypdykk ned i systemet som brukes i Norge når staten vurderer om en medisin er verdt pengene. Altså, om nytten medisinen gir, er verdt pengene den koster.
To ulike løp
Legemiddelverket får tidlig informasjon om hvilke medisiner som er «på vei» til å bli medisinsk godkjent. De kartlegger om dette er en medisin som kan betales via blå resept på folketrygden eller sykehusene, og de lager et notat — et «metodevarsel» — for hver ny medisin.
Se også video: slik blir et legemiddel til. Veien fra idé til produkt
For medisiner på blå resept, er det Legemiddelverket som tar beslutningen om medisinen skal dekkes av myndighetene. Ved en positiv avgjørelse, kan medisinen tas i bruk kort tid etter. Unntaket er dersom Legemiddelverkets godkjenning av medisinen medfører store kostnader, over den såkalte bagatellgrensen/fullmaktsgrensen på 100 millioner kroner årlig fem år etter at medisinen er tatt i bruk. Da er det Stortinget som tar den endelige avgjørelsen, og prosessen tar vesentlig lenger tid.
For medisin betalt av sykehusene, såkalt h-resept, starter prosessen tidligere og er mer omfattende enn for prosessen på blå resept.
Bestillerforum
Notatet fra Legemiddelverket diskuteres i Bestillerforum som er tilknyttet sykehusene, og her bestemmes veien videre for medisinen. Det er de som bestemmer hvilke metodevarsler som skal bestilles og hvilken type dokumentasjon de ønsker fra legemiddelselskapene.
Bestillerforum har månedlige møter for å vurdere metodevarsler. Det er mulighet for både pasientorganisasjoner, produsenter og andre å gi innspill til Bestillerforum i forkant av møtet.
For medisiner som er bedre enn de medisinene som allerede er tilgjengelig, vil det ofte bestemmes at det skal gjøres en grundig vurdering av nytten (effekten av medisinen) opp mot kostnadene (prisen på hva den koster). Ligner medisinen på en annen medisin som allerede er tilgjengelig, kan det bli bestemt at medisinen er «lik nok» til å inngå i en ren priskonkurranse – et anbud.
Les mer om faglig likeverdige legemidler her.
Det er ikke alltid enighet mellom myndighetene, industrien og klinikerne om medisinen er «lik nok» eller hva det faktisk innebærer.
Legemiddelverket
Etter møtet i Bestillerforum, må produsenten — altså legemiddelselskapet — levere det som er bestilt av dokumentasjon, til Legemiddelverket. Dokumentasjonen beviser blant annet hvor effektiv og trygg medisinen er. Dette til tross for at europeiske legemiddelmyndigheter (EMA) allerede har godkjent produktet da de gav markedsføringstillatelse i EU og EØS.
Les også: Kliniske studier – hva er det og hvorfor er det viktig?
Noen ganger kreves mer dokumentasjon enn det som er mulig å fremskaffe. Utviklingsløpet til nye medisiner har endret seg og derfor har også dokumentasjonsgrunnlaget endret seg. Dette gjelder særlig for det som kalles persontilpasset medisin og for avanserte terapier, eller sjeldne diagnoser. Det er færre personer som kan delta i studiene, derfor er det nye måter å gjennomføre kliniske studier på sånn at dokumentasjon om legemiddelet blir fremskaffet, men det utfordrer også den tradisjonelle måten å gjennomføre metodevurderinger på. Dette er utfordrende i Norge og fører ofte til at Legemiddelmyndighetene godtar dokumentasjonen fra EMA for å få medisinen medisinsk godkjent, men det er ofte ikke nok for at myndighetene sier ja til å bruke penger på medisinen. Dokumentasjonen er uansett tidkrevende for legemiddelselskapet å lage, og tidkrevende for Legemiddelverket å gå gjennom.
Dermed vokser også sakskøen hos Legemiddelverket. Her kan det også oppstå uenighet mellom Legemiddelverket og produsenten om dokumentasjonen og nytten av medisinen. Dette er spesielt aktuelt ved små sykdomsområder og/eller ved persontilpasset medisin, hvor det er færre pasienter med i kliniske studier enn det vi tidligere har vært vant til.
Maksimalpris
Etter at produsenten har fått medisinsk godkjennelse, vil dokumentasjonen sendes til Legemiddelverket for vurdering. Selskapet vil også søke Legemiddelverket om en såkalt maksimalpris på medisinen. Av en gruppe på ni europeiske land, er det bestemt av norske myndigheter at denne maksimalprisen er gjennomsnittsprisen av de tre landene med lavest pris – blant landene Sverige, Finland, Danmark, Tyskland, Storbritannia, Nederland, Østerrike, Belgia og Irland.
Samtidig er også produsenten i dialog med sykehusenes innkjøpsorgan Sykehusinnkjøp. Sykehusinnkjøp forhandler med produsentene om rabattert pris på vegne av sykehusene. Under forhandlingene om størrelsen på rabatten, vil det kunne være uenighet om medisinens effekt grunnet nye former for dokumentasjon av dette. Da krever staten enda lavere pris og forhandlingene kan ta ekstra lang tid.
Når prisen er klar og Legemiddelverket har ferdigstilt sin evaluering, vil pristilbudet og Legemiddelverkets vurdering legges frem for sykehusene.
Beslutningsforum
Den endelige avgjørelsen om medisinen kan tas i bruk av norske pasienter, tas av Beslutningsforum, som består av de fire administrerende direktørene i de fire regionale helseforetakene.
Dersom prisen vurderes som for høy i forhold til nytten, kan Beslutningsforum si nei. De kan også velge å ikke ta i bruk medisinen dersom totalkostnaden blir for høy for sykehusene, og fordi de vil prioritere å bruke penger på noe annet. Sykehusbudsjettet skal dekke alt fra dopapir og medisiner, til sykehusbygg og ansattes lønn. Men omtrent 5 % av sykehusbudsjettet går til medisiner.
Anbudsprosess
Dersom Beslutningsforum sier ja, vil medisinen kunne tas i bruk ganske raskt etterpå, med mindre lignende medisiner allerede er i bruk på sykehusene – da må den nye medisinen delta i en anbudskonkurranse før den tas i bruk. Myndighetene arrangerer anbudskonkurranser for hvert terapiområde årlig, så dersom det nylig har blitt gjennomført en anbudskonkurranse, kan det ta opptil 1-2 år før den nye medisinen blir tilgjengelig.
Hele denne prosessen for at et legemiddel kan bli brukt av norske pasienter kan ta måneder og til og med år.
Prioriteringer
Prioriteringsmeldingen omhandler kriterier for prioritering av helseressursene og ble lansert i 2016. Stortinget har bestemt at kriteriet alvorlighet ved sykdom, skal være ett av tre prioriteringshensyn når det vurderes om nye behandlinger kan tas i bruk. De to andre er ressurs og nytte.
Det betyr at gjennomsnittsalderen for pasientgrupper regnes ut og settes opp mot forventede gode leveår i en frisk befolkning. Hvis gjennomsnittsalderen for en pasientgruppe er lav, er betalingsvilligheten relativt høy. Jo høyere gjennomsnittsalderen er, desto lavere blir betalingsviljen.
Et reelt eksempel på dette er da en pasient på 39 år, som er vesentlig yngre enn gjennomsnittspasienten med samme sykdom, ikke fikk tilgang til en potensielt kurerende medisin, fordi hun da ikke passet inn i regnestykket. Hun taper naturligvis flere leveår enn snittpasienten, men så lenge Legemiddelverkets metoder kun legger gruppetenking til grunn – i stedet for metoder mer tilpasset til individuell vurdering – så vil ikke småbarnsmoren få samme overlevelsesmuligheter som mange andre pasienter på sin alder. Kun fordi hun er så uheldig at hun har fått en sykdom «for de eldre.»
Bærekraftig helsetjeneste
Vi er alle tjent med en bærekraftig helsetjeneste, og nye medisiner kan bidra til nettopp det. Samfunnsutviklingen tilsier at det framover må det satses mer på nye legemidler og annen helseteknologi. Kortsiktige besparelser ved ikke å ta i bruk ny teknologi, kan bli dyrt for en helsetjeneste som må omstilles. Også helseminister Bent Høie er klar på at ar klar på at vi trenger å samarbeide om å utvikle ny teknologi for å få en bærekraftig helsetjeneste i fremtiden. Men det hjelper lite å utvikle ny teknologi dersom vi ikke tar den i bruk. Er det riktig at alt fokuset på prioritering legges på legemidler, som altså bare utgjør 5 % av sykehusbudsjettet?
Systemet har blitt evaluert
I november 2021 overleverte Proba samfunnanalyse sin omfattende evalueringsrapport av Systemet for Nye metoder til helseminister Ingvild Kjerkol. Evalueringen hadde to formål:
Evalueringen hadde to formål: Å se på om dagens organisering og saksbehandlingsprosesser i systemet er hensiktsmessig utformet og egnet til å oppnå de fastsatte målene, og å se på om systemet er rustet til å møte fremtidens medisinsk-teknologiske utvikling, herunder utvikling av person-tilpasset medisin.